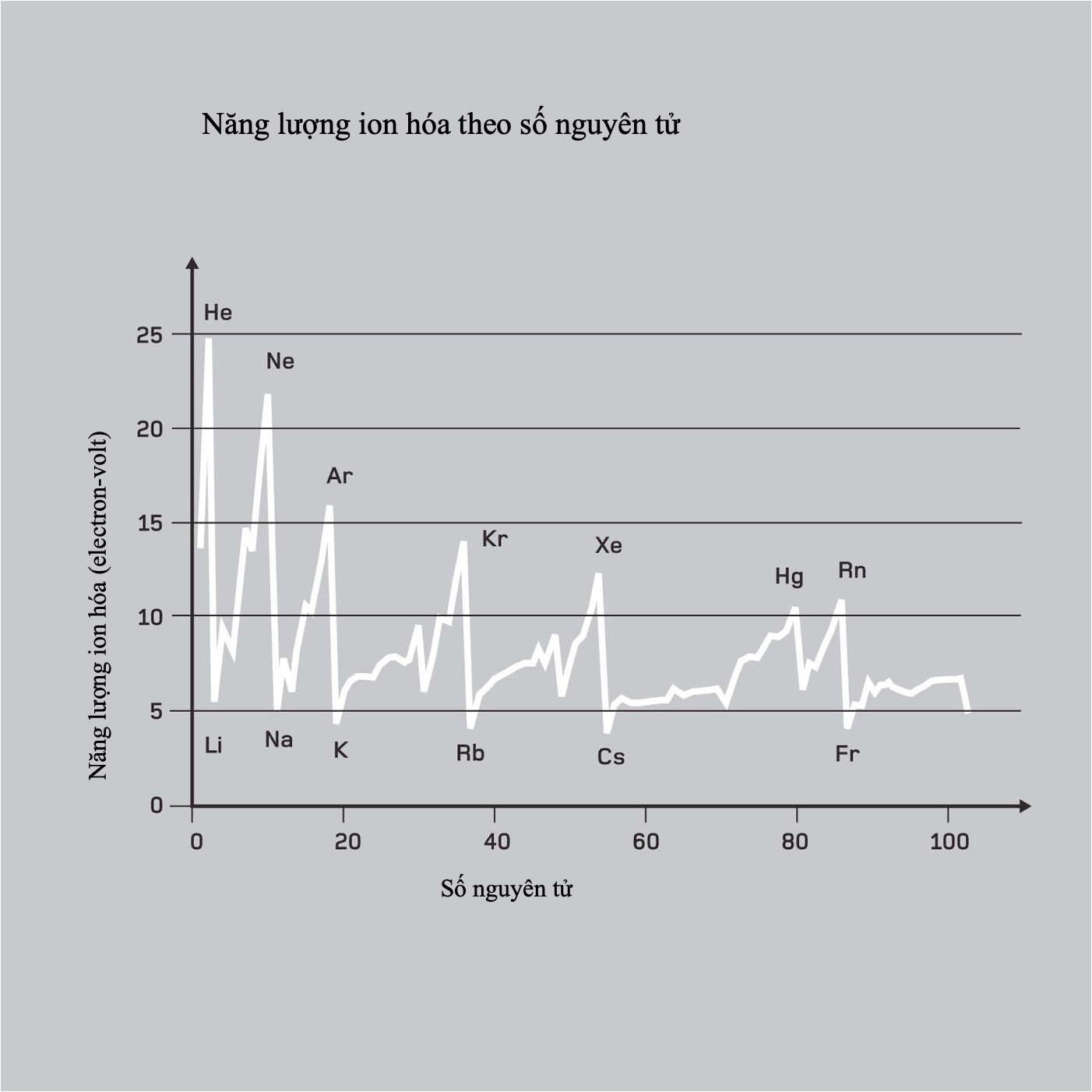
Năng lượng ion hóa
Năng lượng ion hóa là năng lượng cần thiết để loại bỏ một electron ra khỏi một nguyên tử cô lập trong trạng thái khí của nó – năng lượng cần thiết để tạo ra một cation với điện tích dương +1. Không giống độ âm điện, vốn không thể đo trực tiếp, năng lượng ion hóa bậc nhất tương đối dễ xác định bằng thí nghiệm. Hai khái niệm là khác nhau, nhưng có liên hệ với nhau: năng lượng ion hóa càng thấp, thì nguyên tử sẽ càng dễ hình thành cation; độ âm điện càng cao, thì nguyên tử càng dễ hình thành anion.
Trên bảng tuần hoàn, năng lượng ion hóa tăng theo số nguyên tử dọc theo mỗi chu kì, do sự tăng mức bền vững lớp vỏ hóa trị. Dọc xuống mỗi nhóm, năng lượng ion hóa giảm, phần lớn bởi vì các electron thuộc các lớp vỏ phía trong ‘chắn mất’ các electron hóa trị, làm giảm lực hút của chúng với các proton trong hạt nhân. Các xu hướng này ngược lại với độ âm điện, còn các khí trơ không có giá trị cho ái lực electron, thành ra chúng có năng lượng ion hóa rất lớn. Điều này là do sự bền vững của một lớp vỏ hóa trị điền đầy.
Tính kim loại
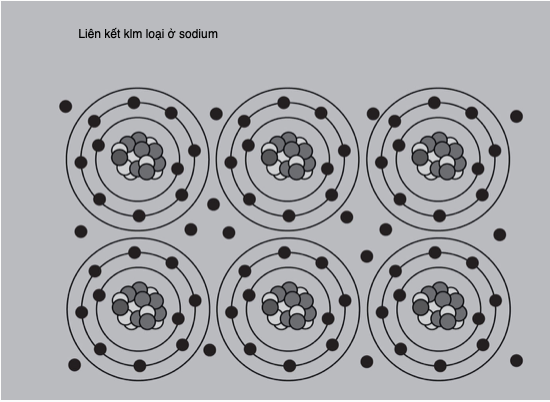
Kim loại là các nguyên tố có các nguyên tử hình thành liên kết kim loại, đem lại cho toàn khối vật liệu những phẩm chất như kì vọng của một kim loại, ví dụ tính dẻo, tính dễ dát mỏng, dẫn nhiệt và dẫn điện. Bất chấp ấn tượng cho bởi bảng tuần hoàn, đường ranh giới giữa kim loại và phi kim không rõ ràng như thế; mặc dù các nguyên tố có vẻ được sắp xếp gọn gàng với các kim loại đối mặt với các phi kim tựa như hai đội quân sắp đánh nhau, nhưng thực tế có nhiều hơn một kim loại bị phân thành phi kim.
Từ trái sang phải theo mỗi chu kì, tính kim loại giảm dần, nhưng không có sự phân chia rõ rệt. Các kim loại ở bên phải block d – thỉnh thoảng được gọi là ‘các kim loại nghèo’ – chỉ có tính kim loại yếu, còn các á kim nương theo đủ loại liên kết hóa học. Dọc xuống mỗi nhóm, tính kim loại tăng, một kiểu hình được dự đoán bởi các xu hướng về năng lượng ion hóa và độ âm điện. Vì năng lượng ion hóa giảm, nên xu hướng hình thành cation tích điện dương tăng lên: điều này giải thích sự biến đổi từ phi kim sang kim loại ở các nhóm 13-15.

Tính dẻo – khả năng kéo một chất thành một sợi thuôn dài – là một tính chất kim loại quan trọng.
Bảng tuần hoàn hóa học tốc hành | Dan Green
Bản dịch của Thuvienvatly.com