Chương 5
Thế giới lượng tử của nguyên tử
Vào cuối thế kỉ 19, các định luật vật lí mô tả hành trạng của những khối vật chất vĩ mô phần lớn đã được xây dựng chắc chắn. Trong số này có các định luật Newton về chuyển động và lực hấp dẫn, chúng có thể dự báo các hiện tượng đa dạng từ sự va chạm của các quả billard, cho đến chuyển động của các hành tinh. Ngoài ra còn có các định luật của nhiệt động lực học, cơ học thống kê của Boltzmann, và sự thống nhất điện học, từ học, và quang học trong các định luật Maxwell về điện từ học. Còn cấu trúc và thế giới bên trong các nguyên tử và phân tử vẫn là một bí ẩn. Có những câu đố chưa có lời giải, ví dụ như nguồn gốc của các vạch phổ nguyên tử sắc nét mà người ta nhìn thấy trong ánh sáng đến từ các sao. Bước sóng của các vạch này trùng khớp với bước sóng do các nguyên tố hóa học phát ra khi đun nóng trên ngọn lửa trong phòng thí nghiệm. Chương này kể lại câu chuyện ra đời của lí thuyết mang tính cách mạng của cơ học lượng tử, song song với những khám phá nổi bật về đặc tính của các nguyên tử.
Một vài manh mối về cấu trúc nguyên tử đã được làm rõ, đặc biệt trong thập niên cuối cùng của thế kỉ 19. Trong số này là tia X có tính đâm xuyên cao (do Wilhelm Röngen khám phá) và sự phóng xạ (do Henri Becquerel khám phá). Các nguyên tử phóng xạ, ví dụ uranium, giải phóng các mảnh vỡ của chúng ở tốc độ cao, tự phát phân rã và phát ra các loại bức xạ ion hóa hay các hạt khác nhau. Một loại phóng xạ, tia gamma, là bức xạ điện từ năng lượng cao. Loại khác bao gồm các hạt alpha tích điện dương, chúng là những thực thể rất bền, và được Ernest Rutherford chứng minh là hạt nhân helium được bắn ra ở tốc độ 10.000 km/s (khoảng 30.000 lần tốc độ âm thanh), và loại thứ ba (hạt beta) là các electron tốc độ cao.
Trái tim của vật chất
Để thăm dò bên trong nguyên tử, Rutherford đi tới ý tưởng sử dụng các hạt alpha nặng làm ‘đạn’ nguyên tử. Vào năm 1912, cùng với Ernest Marsden và Hans Geiger, ông bắn các hạt alpha vào một lá vàng mỏng (Hình 12). Đa phần các hạt nhanh đó cày thẳng qua hàng triệu nguyên tử vàng mà chúng gặp phải, mãnh liệt xô đẩy các electron nhẹ. Nhưng thi thoảng các hạt alpha bị tán xạ qua góc nhỏ, số ít bị lệch những góc lớn hơn, và một tỉ lệ nhỏ còn bị tán xạ lùi. Nói theo lời Rutherford: ‘cứ như là bạn bắn một quả đạn 15 inch vào một tờ giấy mỏng và nó dội ngược lại và đập vào bạn’. Thí nghiệm chứng tỏ rằng nằm tại tâm nguyên tử là một hạt nhân bé xíu, tích điện dương, và khối lượng lớn. Thỉnh thoảng một hạt alpha có thể đập trúng trực diện một hạt nhân vàng, chịu lực đẩy tĩnh điện mạnh của nó, và dội lại. Hạt nhân một proton của nguyên tử hydrogen có đường kính 10-15 m, nhỏ hơn nguyên tử khoảng 100.000 lần. Các nguyên tử chủ yếu là trống rỗng. Giả sử phóng to một nguyên tử hydrogen lên bốn nghìn tỉ lần bằng kích cỡ sân vận động Wembley ở London, thì hạt nhân của nó sẽ chừng bằng một hạt đậu.
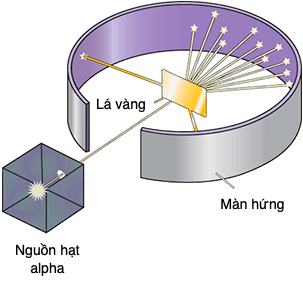
Hình 12. Thí nghiệm của Rutherford làm tán xạ hạt alpha khỏi các nguyên tử vàng đã dẫn tới khám phá hạt nhân nguyên tử.
Hạt nhân nhỏ bé, khối lượng lớn, và tích điện dương, thế nó được làm bằng gì? Một trăm năm trước đây, các thí nghiệm hóa học của Dalton đã làm rõ các tỉ số nguyên đơn giản giữa trọng lượng nguyên tử của các nguyên tố, tính theo đơn vị trọng lượng của nguyên tử hydrogen. Kết quả dự đoán rằng hạt nhân được cấu tạo từ những viên gạch cấu trúc proton, hạt nhân của nguyên tử hydrogen. Vào năm 1919, Rutherford xác nhận dự đoán này khi cho đánh bật proton ra khỏi nitrogen, một lần nữa lại sử dụng hạt alpha.
Việc khám phá rằng hạt nhân chứa các proton làm nảy sinh một câu hỏi sâu sắc hơn nữa. Khi di chuyển theo bảng tuần hoàn, trọng lượng nguyên tử của mỗi nguyên tố tăng lên nhanh hơn nhiều so với số nguyên tử của nó. Đối với hydrogen, số nguyên tử và trọng lượng đều bằng 1. Ở helium (số nguyên tử 2), trọng lượng lớn gấp bốn lần. Rồi đến nguyên tố 92, uranium, trọng lượng nguyên tử gấp hydrogen đến 238 lần. Phải có thứ gì đó tạo nên độ hụt giữa điện tích và khối lượng trong hạt nhân, và Rutherford dự đoán rằng, ngoài proton ra, phải có mặt những hạt nặng khác nữa. Ông gọi các hạt này là neutron vì chúng không mang điện. James Chadwick đã tìm thấy neutron vào năm 1932 khi ông bắn hạt alpha vào các nguyên tử beryllium và đánh bật neutron ra khỏi chúng. Mỗi neutron cân nặng hơn proton một phần mười phần trăm; nhưng ngoài sự trung hòa điện của nó thì hai hạt là giống nhau. Proton và neutron trong hạt nhân được gọi là nucleon (Hình 13). Các nguyên tố có cùng số proton trong hạt nhân của chúng đều có hóa tính giống nhau, nhưng chúng có thể có số lượng neutron khác nhau, biến chúng thành các đồng vị của nguyên tố đó. Ví dụ, helium-4 có hai proton và hai neutron trong khi helium-3 có hai proton và chỉ một neutron.
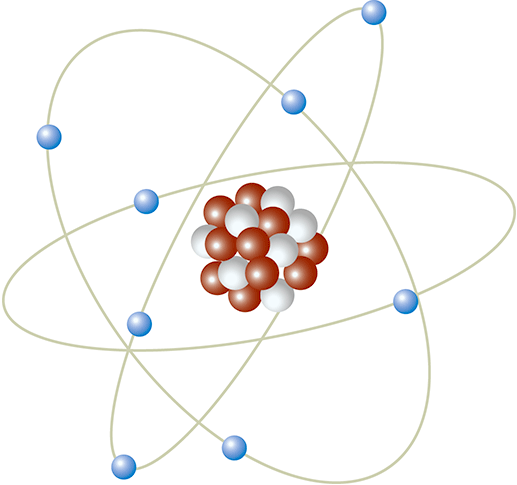
Hình 13. Hình biểu diễn một nguyên tử cho thấy các neutron và proton kết tập với nhau trong hạt nhân nguyên tử, vây xung quanh là electron. (Lưu ý: hình ảnh hạt nhân đã được phóng to 100.000 lần so với các quỹ đạo electron; nếu vẽ đúng tỉ lệ, bạn sẽ không nhìn thấy hạt nhân.)
Hạt nhân được giữ lại với nhau như thế nào? Với khoảng 100 proton chen chúc vào một thể tích tí xíu của nó, lực đẩy tĩnh điện tương hỗ trong hạt nhân là vô cùng lớn và một lực khác, lực hạt nhân mạnh, liên kết toàn đám hạt lại với nhau. Lực mạnh lớn gấp nhiều lần so với lực điện, và hoạt động trên một khoảng cách ngắn hơn nhiều, chừng 10-15 mét. Ta có thể mường tượng lực này mạnh bao nhiêu bằng cách so sánh nó với sức chặt mà mỗi electron liên kết với nguyên tử. Đơn vị năng lượng tiện dùng ở cấp vi mô của vật chất là electron volt, hay eV. Công cần thiết để di chuyển một electron qua một thế năng điện, nói ví dụ giữa hai điện cực của một cục pin ‘AA’ 1,5 volt, là 1,5 eV. (Có 6,25 ´ 1018 eV trong một Joule). Để loại một electron ra khỏi nguyên tử, cần năng lượng vào khoảng 15 eV, năng lượng này có thể được cấp dễ dàng bởi 10 cục pin cỡ AA. Nhưng để loại một proton ra khỏi hạt nhân sẽ cần năng lượng khoảng 10 MeV, tương đương với bảy triệu cục pin. Giả sử bạn có thể tiếp cận hạt nhân nguyên tử với một cặp nhíp khỏe và kẹp một neutron ra, thì lực cần thiết sẽ tương đương với lực nâng một cái va li nặng.
Lượng tử hóa nguyên tử
Khám phá về hạt nhân nguyên tử đã đưa đến bức tranh nguyên tử là một hình ảnh thu nhỏ của hệ mặt trời, không khác mấy với Hình 13, trong đó hạt nhân nằm ở trung tâm giống như Mặt Trời, với các electron quay xung quanh giống như các hành tinh. Tuy nhiên, người ta nhanh chóng nhận ra rằng nếu các electron hành xử theo lối cổ điển, thì các nguyên tử sẽ nhanh chóng bức xạ hết toàn bộ năng lượng của chúng và co sụp dưới lực hút giữa các điện tích dương và âm. Vậy thì sự bền vững của các nguyên tử do đâu mà có?
Khái niệm chủ chốt cần thiết để tìm hiểu sự bền vững nguyên tử đã được đề xuất hồi năm 1900, nhưng trong một lĩnh vực khác của vật lí học – nghiên cứu về bức xạ do các vật nóng phát ra. Trong khi nghiên cứu bức xạ nhiệt, nhà vật lí Đức Max Planck đã có một ý tưởng căn bản: năng lượng bức xạ phải bị lượng tử hóa. Planck đề xuất rằng năng lượng của trường điện từ được bó lại thành những gói rời rạc, hay các lượng tử, thay vì tạo ra những con sóng với dải năng lượng liên tục gần xuống zero, như lí thuyết của Maxwell dự đoán. Năng lượng của mỗi lượng tử Planck tỉ lệ thuận với tần số bức xạ, thế nên mỗi lượng tử ánh sáng lam tần số cao, chẳng hạn, mang năng lượng nhiều gấp đôi mỗi lượng tử của ánh sáng đỏ. Hằng số tỉ lệ, h, là một hằng số cơ bản của tự nhiên, được gọi là hằng số Planck. Nó có cùng đơn vị với động lượng của một vật quay, hay moment động lượng. Hằng số Planck là một con số rất nhỏ và xác định những bước nhảy nhỏ nhất mà tự nhiên thực hiện, hay lượng tử tác dụng.
Chẳng mấy chốc sau đề xuất mang tính cách mạng của Planck, Einstein đã mở rộng ý tưởng lượng tử hóa bằng cách chỉ ra rằng ánh sáng truyền đi trong không gian gồm các hạt, gọi là photon, mang những gói năng lượng rời rạc. Ý tưởng này giải thích cho một hiện tượng nổi tiếng gọi là hiệu ứng quang điện trong đó các kim loại như kẽm có thể giải phóng electron khi chiếu ánh sáng tử ngoại tần số cao lên chúng. Để tróc một electron ra khỏi kim loại, phải có một năng lượng tối thiểu được phân phối đến nó, và tần số cao của photon đem lại năng lượng này. Nếu tần số ánh sáng dưới một giá trị tới hạn thì chẳng có electron nào bật ra cho dù nguồn sáng có cường độ mạnh đến bao nhiêu.
Nhà vật lí Đan Mạch Niels Bohr đã áp dụng sự lượng tử hóa năng lượng cho cấu trúc điện tử của nguyên tử. Ông nêu lí thuyết rằng mỗi electron chuyển động trong một quỹ đạo xung quanh hạt nhân chỉ có thể chiếm giữ những quỹ đạo rời rạc với các giá trị số nguyên (1, 2, 3,…) lần moment động lượng, theo đơn vị h/2p. Các giá trị số nguyên ấy được gọi là các số lượng tử chính. Năng lượng của các quỹ đạo khác nhau tạo thành một cái thang rời rạc gồm các trạng thái được phép với các thanh thang cách nhau không đều (Hình 14). Quy tắc lượng tử nói rằng mỗi electron trong nguyên tử chỉ được phép nằm ở trên các thanh thang, không bao giờ nằm lưng chừng giữa chúng. Nó có thể nhảy lên một thanh cao hơn (một trạng thái kích thích) bằng cách hấp thụ một lượng tử năng lượng bằng với hiệu năng lượng giữa hai thanh, hoặc rơi xuống một thanh năng lượng thấp hơn bằng cách phát ra một photon có năng lượng và tần số nhất định. Thanh thấp nhất trên thang năng lượng được gọi là trạng thái cơ bản, và, do không có trạng thái nào bên dưới nó, các electron bị ngăn cản lao vào hạt nhân; đây chính là chỗ khiến nguyên tử bền vững. Ngoài việc giải thích sự bền vững của nguyên tử, mô hình Bohr còn phân giải câu hỏi đã tồn tại dai dẳng về nguồn gốc của các vạch sắc nét trong quang phổ nguyên tử. Khi ông sử dụng lí thuyết này dự đoán bước sóng quan sát thấy của quang phổ vạch hydrogen, mô hình nguyên tử của ông lập tức thu về một thắng lợi lớn.
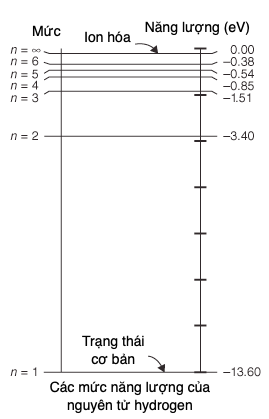
Hình 14. Thang mức năng lượng lượng tử của nguyên tử hydrogen cho thấy một dải vạch ngang. Năng lượng là các con số âm do chúng thể hiện năng lượng cần thiết để loại một electron từ mức đã cho ra vô cùng. Các số lượng tử chính được kí hiệu bằng n.
Sóng và hạt
Tự nhiên áp đặt những quy tắc lượng tử chặt chẽ lên vật chất. Mỗi electron không thể có năng lượng bất kì trong nguyên tử, mà nó bị ràng buộc với một thang năng lượng lượng tử rời rạc. Làm thế nào hiểu cho đúng hành trạng kì lạ này? Mấu chốt là nhận ra rằng các hạt vi mô có các đặc trưng dạng sóng. Mọi kiểu sóng đều có những đặc trưng cơ bản như bước sóng (khoảng cách giữa hai đỉnh sóng liên tiếp) và biên độ (độ cao của sóng). Chúng có thể truyền tự do trong không gian dưới dạng sóng chạy, hoặc sóng đứng tại chỗ, sóng dừng, ví dụ như các dao động của một sợi dây đàn ghita. Các electron trong nguyên tử hành xử giống như các sóng dừng.
Tính chất tinh túy của các sóng là giao thoa. Nếu bạn ném đồng thời hai cục đá xuống một mặt hồ tĩnh lặng, thì các gợn tròn từ mỗi chấn động lan tỏa ra và cắt nhau. Khi các sóng gặp nhau, mỗi sóng cộng gộp với sóng kia (gọi là chồng chất tuyến tính). Khi hai đỉnh sóng gặp nhau, chúng cộng lại thành một đỉnh nhô cao gấp đôi (giao thoa tăng cường); khi hai hõm sóng gặp nhau, chúng tạo ra một hõm sóng sâu gấp đôi. Nếu một đỉnh sóng và một hõm sóng gặp nhau, thì triệt tiêu nhau nên bề mặt nước phẳng lặng (giao thoa triệt tiêu). Ánh sáng biểu hiện mô hình giao thoa này, và vào năm 1801 Thomas Young đã thực hiện thí nghiệm hai khe nổi tiếng của ông (Hình 15), khẳng định chắc chắn bản chất sóng của ánh sáng. Khi chiếu ánh sáng lên một cặp khe song song sít nhau cắt trên một màn chắn, các sóng tỏa ra phía bên kia tạo ra một kiểu dải sáng và tối của sự giao thoa tăng cường và triệt tiêu.
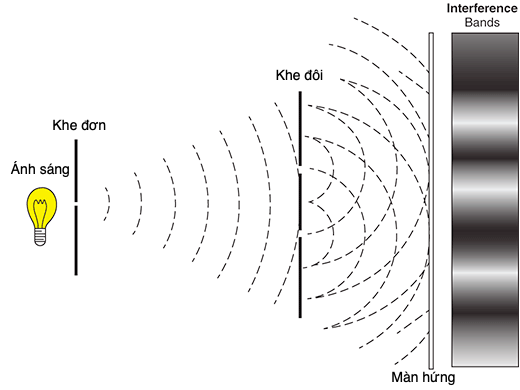
Hình 15. Thí nghiệm hai khe của Thomas Young cho thấy các dải vân giao thoa sáng và tối được tạo ra bởi sự giao thoa tăng cường và triệt tiêu của các sóng ló ra từ hai khe.
Sau giải thích của Einstein về hiệu ứng quang điện theo khái niệm photon, vấn đề trở nên sáng tỏ là ánh sáng vừa có đặc trưng dạng hạt vừa có đặc trưng dạng sóng. Sự lưỡng tính sóng-hạt là (và vẫn là) một khái niệm khó tiêu hóa đối với chúng ta; nhưng bằng chứng cho sự tồn tại của các photon và dải vân giao thoa dạng sóng của Young là không thể chối cãi. Vào năm 1924, một ý tưởng xảy đến với một chàng quý tộc Pháp trẻ tuổi, hoàng tử Louis de Broglie. Nếu ánh sáng có bản chất lưỡng tính, vậy tại sao những hạt nhỏ nhất của vật chất lại không có đặc trưng dạng sóng kia chứ? De Broglie đã định nghĩa bước sóng của một hạt lượng tử, gọi là bước sóng de Broglie ldB, theo động lượng mv (khối lượng ´ vận tốc) của nó:

Thang kích cỡ mà trên đó các hiệu ứng lượng tử dạng sóng trở nên quan trọng được cố định bởi độ lớn của hằng số Planck ở tử thức. Động lượng của hạt xuất hiện ở mẫu thức, dự đoán rằng một miếng vật chất càng nặng và/hoặc tốc độ của nó càng lớn, thì bước sóng lượng tử càng nhỏ. Điều này có nghĩa là các vật thể vĩ mô, ví dụ như quả billard, có bước sóng de Broglie nhỏ đến mức không đáng chú ý. Nhưng ở cấp nguyên tử thì bản chất sóng của vật chất là trọng tâm.
De Broglie hình dung các sóng tương ứng với các hạt chuyển động tự do. Thế nhưng, khi nhìn dưới dạng sóng dừng, chúng đem lại nhận thức mới cho cách các quỹ đạo electron của Bohr bị lượng tử hóa. Nếu người ta hình dung việc bẻ cong một sóng elecron thành một vòng tròn vây xung quanh hạt nhân, thì chỉ có những cách nhất định để làm như vậy sao cho hai đầu của nó nối liền mượt mà với nhau. Điều kiện toán học là chu vi quỹ đạo phải chứa đúng số nguyên lần bước sóng. Nếu bước sóng hoặc chu vi chỉ lệch một chút khỏi điều kiện này, thì sóng electron sẽ không nối mượt và sẽ nhanh chóng mất đồng bộ và triệt tiêu. Đây là lí do vì sao các electron không thể nằm trong các khe trống giữa các thanh nganh trong thang năng lượng lượng tử.
Nguyên lí bất định
Trong cơ học cổ điển, các định luật Newton về chuyển động mô tả hoàn toàn đầy đủ chuyển động của một hạt vĩ mô trong một trường lực. Cả vị trí lẫn động lượng của một chất điểm được xác định rạch ròi về mặt toán học và là những đại lượng độc lập, và quỹ đạo của nó được xác định rõ nét trong không-thời gian. Nhưng điều này không đúng ở cấp lượng tử, trong đó các hạt chuyển động từ vị trí này sang vị trí khác theo mỗi lộ trình khả dĩ trong không-thời gian. Thành ra sẽ vô nghĩa nếu nghĩ tới việc cố định một vật thể lượng tử trong một vùng không gian nhỏ hơn bước sóng của nó. Hơn nữa, bước sóng của một vật lượng tử tỉ lệ nghịch với động lượng của nó theo công thức de Broglie, và các biến vị trí và động lượng không phải là độc lập. Một bước sóng vật chất lớn hàm ý một động lượng nhỏ, và ngược lại. Các biến vị trí và động lượng tạo thành những cặp đặc biệt, gọi là các biến bổ sung.
Vào năm 1926, nhà vật lí Đức Werner Heisenberg đã xác định lí thuyết hoàn chỉnh đầu tiên về cơ học lượng tử (gọi là cơ học ma trận, liên quan đến những đối tượng toán học gọi là ma trận). Trong lí thuyết này, ông tập trung vào ý nghĩa của việc tiến hành một phép đo trên một hệ lượng tử và kết luận rằng kiến thức mà chúng ta có thể thu được về nó vốn bị hạn chế bởi tự nhiên, với độ chính xác chẳng liên quan gì với các sai sót hay hạn chế trong trang thiết bị đo. Một thực thể lượng tử không tự nó biết nó ở đâu và nó đang chuyển động nhanh bao nhiêu hay nó đang chuyển động theo hướng nào – thế giới lượng tử vốn dĩ là bất định. Heinsenberg đi tới ý tưởng chủ chốt, nguyên lí bất định, thừa nhận rằng chúng ta có thể biết hoặc là một vật lượng tử đang ở đâu hoặc nó đang chuyển động đi đâu, nhưng chúng ta không thể biết đồng thời cả hai. Nguyên lí bất định là nền tảng cho toàn bộ cơ học lượng tử và nó cho chúng ta biết rằng các thực thể lượng tử không phải thuần túy là hạt hay thuần túy là sóng.
Nguyên lí bất định liên hệ độ chuẩn xác hay sai số (kí hiệu bằng D) về vị trí của một hạt (Dx) với sai số về động lượng của nó (Dp), sao cho tích của hai sai số lớn hơn hoặc bằng hằng số Planck/4p:
Dx.Dp ³ h/4p
Công thức này vận hành như thế nào? Giả sử chúng ta muốn đo vị trí và tốc độ của một electron. Ta có thể chiếu một ánh sáng lên electron đó và tìm xem nó ở đâu và nó chuyển động như thế nào bằng ánh sáng mà nó tán xạ về phía chúng ta. Tuy nhiên, electron đó có khối lượng rất nhỏ và, để tránh làm nhiễu loạn nó nhiều quá, ta cần chiếu một ánh sáng mờ mờ lên nó thôi. Tuy nhiên, electron đó phải tán xạ ít nhất một photon thì nó mới được nhìn thấy; khi nó làm thế, có một sự trao đổi năng lượng và động lượng. Do đó, photon không thể tránh khỏi truyền động lượng cho electron, một tương tác về cơ bản khiến ta không thể quan sát một hạt mà không làm nhiễu nó. Thế các lựa chọn là gì? Ta có thể chọn làm nhiễu electron càng ít càng tốt và tiến hành một phép đo chính xác hơn về động lượng của electron bằng cách sử dụng một photon bước sóng dài năng lượng thấp, như minh họa ở Hình 16. Nhưng khi ta làm thế, vì ta không thể cố định một vật trong không gian với độ chuẩn xác nhỏ hơn bước sóng của ánh sáng được sử dụng (trong trường hợp này lớn), nên phép đo của chúng ta về vị trí trở nên bất định. Hoặc là, ta có thể chọn làm giảm sai số khi đo vị trí của electron bằng cách sử dụng một photon bước sóng ngắn năng lượng cao (ví dụ một photon tia gamma), như minh họa ở bên phải Hình 16. Nhưng, với một photon tia gamma năng lượng cao, ‘cú hích’ mà electron nhận được bây giờ quá lớn nên phép đo động lượng trở nên quá bất định. Nguyên lí bất định khiến người ta không thể thực hiện đồng thời các phép đo vị trí và động lượng, đến mức độ chính xác cao tùy ý.
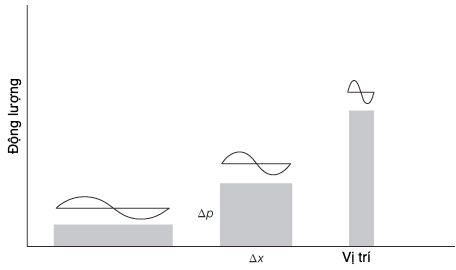
Hình 16. Minh họa nguyên lí bất định Heisenberg, trong đó lượng tử tác dụng bị ‘nén’ theo những cách khác nhau. Độ bất định khi đo động lượng của một hạt, Dp, tỉ lệ nghịch với độ bất định vị trí của nó, Dx, sao cho diện tích trong không gian động lượng-vị trí (được biểu diễn bằng các hình chữ nhật tô màu xám) tỉ lệ với hằng số Planck. Ánh sáng bước sóng dài, trung bình, và ngắn dùng để đo một hạt lượng tử được biểu diễn trên mỗi hình chữ nhật.
Nguyên lí bất định rất quyền năng. Trong số nhiều hệ quả quan trọng của nó là tính chất nói rằng khi một hạt lượng tử bị định xứ chặt trong không gian thì nó chịu những thăng giáng lớn về động lượng và, do đó, động năng, gọi là năng lượng điểm zero. Các thực thể lượng tử liên tục thăng giáng trong trạng thái năng lượng thấp nhất của chúng. Nguyên lí bất định cấm vật chất đạt tới độ không tuyệt đối do bởi, nếu đạt tới, thì các hạt sẽ có vị trí chính xác trong không gian, và điều đó bị cấm.
Khái niệm về năng lượng định xứ hóa lượng tử còn giúp chúng ta hiểu được sự bền vững của nguyên tử. Hãy hình dung việc xây dựng một nguyên tử hydrogen bằng cách mang một electron và một proton từ vô cực lại với nhau. Điểm xuất phát là hai hạt cách nhau rất xa, và điểm cuối là chuyển động ràng buộc lượng tử của một electron trong trường lực tĩnh điện của hạt nhân proton của nó. Khi electron tiến đến gần proton, động năng mà nó thu từ trường tĩnh điện khiến nó loạng choạng, chao đảo dữ dội xung quanh proton dưới dạng một quả cầu dao động nhòe nhoẹt. Thoạt đầu, quả cầu ấy lớn, nhưng khi electron bức xạ dần năng lượng của nó thì quả cầu ấy co lại, và nó càng lúc càng gần vùng phụ cận của proton, chiếm giữ một thể tích chặt chẽ được xác định bởi cỡ Dx. Vì Dx nhỏ dần, nên độ phân tán động lượng Dp của nó phải tăng tương ứng theo nguyên lí bất định. Thành ra động năng của electron tăng, đối ngược với sự co lại. Cuối cùng, các tác dụng cạnh tranh của lực hút tĩnh điện và năng lượng định xứ hóa lượng tử cân bằng nhau khi electron rơi vào trạng thái cơ bản năng lượng tối thiểu của nó. Sự thỏa hiệp của tự nhiên là tạo ra các nguyên tử bền vững với thang lượng tử của các mức năng lượng điện tử.
Giải thích thế giới lượng tử
Không bao lâu sau khi Heisenberg công bố lí thuyết ma trận của ông, nhà vật lí Áo Erwin Schrödinger công bố một cách tiếp cận khác, nó được xây dựng trên một phương trình mô tả động lực học của các hạt lượng tử dạng sóng chuyển động trong một trường lực. Phương trình Schrödinger tương tự như các phương trình sóng cổ điển chi phối cách các gợn sóng chuyển động trên mặt hồ hay sóng âm truyền đi trong không khí. Nó là phương trình cơ bản của thuyết lượng tử và là cái tương đương với động lực học Newton trong thế giới vi mô. Các hình thức Heisenberg và Schrödinger, mặc dù khác nhau về diện mạo, nhưng là tương đương với nhau về mặt vật lí.
Các nghiệm cho phương trình Schrödinger được gọi là các hàm sóng, và chúng mô tả các sóng được kí hiệu bằng chữ Ψ. Điều này lập tức làm phát sinh câu hỏi nên hiểu hàm sóng như thế nào cho đúng. Mọi sóng đều có các giá trị dương và âm (ví dụ, sóng biển có trồi lên trên hoặc hụp xuống bên dưới mặt nước biển). Vậy thì, nếu một hạt lượng tử được biểu diễn bằng một hàm sóng, thì người ta nên giải thích như thế nào về các giá trị âm? Max Born quả quyết rằng bình phương của hàm sóng Ψ2 (không bao giờ âm) biểu diễn xác suất (và không phải sai số) tìm thấy hạt trong một vùng không gian nhất định.
Một đặc điểm căn bản thứ hai của phương trình Schrödinger là nó tuyến tính. Trong một phương trình tuyến tính, tổng của hai hoặc nhiều nghiệm tự nó là một nghiệm. Điều này có nghĩa là tổng của các hàm sóng cũng là một hàm sóng biểu diễn một trạng thái hỗn hợp cho phép một hệ lượng tử ở nhiều hơn một trạng thái cùng lúc. Mỗi trạng thái lượng tử có thể diễn tiến độc lập, như thể chẳng có trạng thái khác nào ở đó. Đặc điểm này làm phát sinh một đặc điểm kì lạ và độc đáo của thế giới lượng tử, sự chồng chất lượng tử. Khi một hệ lượng tử ở trong sự chồng chất của các trạng thái, thì không thể nào định rõ các đặc trưng vật lí của nó được.
Sự chồng chất lượng tử có thể giúp chúng ta hiểu được hành trạng kì lạ của cách electron nguyên tử có thể nhảy giữa các thanh ngang trên thang lượng tử, dường như biến mất khỏi một mức (trạng thái A) và xuất hiện ở mức kia (trạng thái B), mà không đi qua bất kì trạng thái trung gian nào. Khi nguyên tử thực hiện một bước nhảy lượng tử từ trạng thái A sang trạng thái B, electron tương tác trong khoảnh khắc với một photon. Trong thời gian đó, hàm sóng của các trạng thái ban đầu và cuối cùng chồng chất, và người ta nói electron ở trong một sự chồng chất trạng thái. Sự chồng chất là một hỗn hợp của hai trạng thái: electron ở trạng thái A, và electron ở trạng thái B. Khi chuyển tiếp nguyên tử đó diễn ra, hàm sóng cho trạng thái A trở nên yếu đi, còn hàm sóng của B trở nên mạnh hơn cho đến cuối cùng thì chỉ còn riêng trạng thái B. Một tương tự thô cho tình huống này là ‘tiếng rít’ ngắn ngủi được tạo ra bởi một nhạc cụ khí, khi nó đảo giữa hai mode dao động.
Có một thí nghiệm chủ chốt tiến thẳng vào tâm của nguyên lí chồng chất: thí nghiệm hai khe của Young, được thực hiện với các hạt thay vì ánh sáng. Thí nghiệm này là một ưa thích của Richard Feynman, ông nói: ‘trên thực tế nó chứa đựng bí ẩn duy nhất… của toàn bộ cơ học lượng tử’. Hãy nhìn lại thí nghiệm ở Hình 15, sử dụng một chùm electron chiếu vào một màn kim loại có hai khe hẹp song song. Ở phía xa bên kia là một màn thủy tinh. Nếu electron đi qua hai khe, chúng sẽ đập vào màn thủy tinh, và hiện thân dưới dạng những lóe sáng bé xíu. Nếu che đi một trong hai khe, thì hình ảnh lóe sáng trên màn thủy tinh được tìm thấy là đều, với các electron đi qua khe mở và đập trúng điểm mục tiêu trên màn phía sau như thể chúng là những viên đạn tí hon. Nếu bây giờ mở khe bị che ra, thì electron có thể đi qua cả hai khe và hình ảnh các lóe sáng trên màn thủy tinh thay đổi rất nhiều. Hình ảnh đồng đều bây giờ chuyển thành một hình ảnh dạng sóng, với các dải giao thoa tăng cường và triệt tiêu. Điều quan trọng là các electron bây giờ bị cấm đi tới những vùng nhất định trên màn, chúng vốn dĩ dễ dàng đập trúng những nơi đó khi chỉ có một khe mở. Kết quả kịch tính này hoàn toàn mâu thuẫn với bức tranh tinh thần của chúng ta rằng các electron hành xử giống như những viên đạn tí hon; nếu electron giống như các viên đạn, vậy tại sao việc mở khe thứ hai làm ảnh hưởng đến các electron đi qua khe thứ nhất?
Thí nghiệm này có thể được xem xét ở một tầng sâu hơn. Tốc độ bắn của súng electron bây giờ được chỉnh xuống sao cho chỉ có một electron bay qua thiết bị tại mỗi thời điểm. Với cả hai khe đều mở, vị trí electron đập lên màn thủy tinh được ghi lại và, theo thời gian, dần dần tạo nên một hệ vân dạng sóng, giống hệt như một trong các thí nghiệm trước đây, khi hai khe đều mở. Nhưng làm thế nào như vậy được khi mà chỉ có một electron trong thiết bị? Phải chăng electron nhòa ra và bằng cách nào đó qua cả hai khe đồng thời để giao thoa với chính nó? Nếu chúng ta cố nhận ra electron đi qua khe nào, nói ví dụ bằng cách làm tán xạ một photon lên nó, tác dụng đo gây nhiễu trạng thái của electron và hình ảnh trên màn thủy tinh lập tức chuyển về hình ảnh đều.
Hãy tóm tắt hành trạng kì lạ này. Nếu chẳng có ai đang quan sát electron, thì rõ ràng nó có thể đi qua cả hai khe cùng lúc. Trong trường hợp đó, hàm sóng electron ở trong sự chồng chất của các trạng thái: cụ thể là, electron đi qua khe thứ nhất, và cũng electron đó đi qua khe thứ hai. Còn nếu electron được quan sát, thì hàm sóng của nó được nói là suy sụp thành một trạng thái tương ứng với việc nó chỉ qua một khe. Như vậy, việc nhìn và không nhìn vào electron gây ra hai thí nghiệm khác nhau, mỗi thí nghiệm đem lại một kết quả khác nhau.
Khái niệm về sự suy sụp của hàm sóng là trọng tâm đối với ‘cách hiểu Copenhagen’ của cơ học lượng tử, một tập hợp ý tưởng do Niels Bohr dẫn dắt vào năm 1927. Tên gọi phát sinh từ nơi có viện nghiên cứu của Bohr. Bohr công nhận rằng hiểu biết của chúng ta về thế giới lượng tử chỉ đến từ các phép đo do chúng ta thực hiện ở cấp vĩ mô, sử dụng trang thiết bị thí nghiệm tiêu biểu. Do một hệ lượng tử bị nhiễu khi các phép đo được tiến hành trên nó, nên sẽ vô nghĩa nếu hỏi hạt lượng tử đang làm gì khi không có ai quan sát nó. Điều duy nhất người ta có thể làm là tính các xác suất để một hệ lượng tử chiếm giữ những trạng thái nhất định. Thời khắc nhà quan sát thực hiện phép đo, hệ bị ép phải suy sụp vào một trạng thái duy nhất, ngay lúc đó hệ ‘quyết định’ nó ở trong trạng thái nào. Einstein không bao giờ hài lòng với nền tảng xác suất của cách hiểu Copenhagen và, trong một loạt trao đổi nổi tiếng với Bohr, ông tuyên bố nổi tiếng rằng ‘Chúa không chơi xúc xắc’, và Bohr đáp lại: ‘Einstein, đừng có bảo Chúa phải làm gì.’ Tuy nhiên, cho dù chúng ta chọn cách hiểu hàm sóng như thế nào, phương trình Schrödinger vẫn vượt qua các phép kiểm tra thực nghiệm chính xác.
Thế nhưng ngay cả Schrödinger cũng chẳng hài lòng với lí thuyết của ông hay cách hiểu Copenhagen. Để minh họa cho những điều vô lí nảy sinh, ông ngụy tạo một thí nghiệm giả tưởng gọi là con mèo của Schrödinger. Ông hình dung việc đặt một con mèo vào trong một cái hộp kín, cùng với một nguyên tử phóng xạ và một dụng cụ giải phóng một chất khí độc chết chóc ngay thời khắc nguyên tử phân rã, một tác dụng sẽ giết chết con mèo. Sau một thời gian nhất định, xác suất để nguyên tử đó đã phân rã là 50 phần trăm, và nguyên tử đó ở trong sự chồng chất của hai trạng thái: chưa phân rã và đã phân rã. Nếu nguyên tử đã phân rã, thì chất độc đã được giải phóng và con mèo đã chết. Ngược lại thì nguyên tử vẫn nguyên vẹn, và con mèo còn sống. Vì cái hộp đóng kín, nên ta chẳng có cách nào biết được con mèo còn sống hay đã chết, và thí nghiệm mời chúng ta xem xét sự chồng chất của hai trạng thái của nguyên tử đã ‘rò rỉ’ và ảnh hưởng đến cái đựng bên trong hộp, kể cả con mèo, nó cũng phải ở trong sự chồng chất của sống và chết. Nếu cách hiểu Copenhagen là đúng, thì mọi thứ vẫn u minh cho đến khi một nhà quan sát nhìn vào bên trong cái hộp. Vào lúc này sự chồng chất suy sụp và con mèo trở nên hoặc chết hoặc còn sống. Sự vô lí nằm ở thực tế chúng ta biết con mèo trên thực tế hoặc là chết hoặc là sống, chứ không bao giờ cả hai cả.
Trạng thái kì lạ này đã khuyến khích một vài cách lí giải khác của cơ học lượng tử. Một trong số này được nêu ra vào những năm 1950 bởi Hugh Everett và được gọi là ‘cách hiểu đa thế giới’. Theo cách hiểu này, không có sự suy sụp của hàm sóng, mà thay vậy Everett thừa nhận rằng thứ gì có thể xảy ra đều thật sự xảy ra. Điều này có nghĩa là khi nguyên tử phóng xạ và con mèo tiến vào một trạng thái chồng chất, thực tại vật chất chia tách thành hai phiên bản tách biệt và song song: trong một phiên bản con mèo sống và trong phiên bản kia con mèo chết. Nếu mở rộng kịch bản này để bao hàm toàn bộ mọi tác dụng đo khả dĩ trong vũ trụ, thì thực tại vật chất chia tách thành vô số vũ trụ tách biệt, một khái niệm đã khuyến khích các nhà vũ trụ học đề xuất về đa vũ trụ. Đa vũ trụ là một số lượng lớn các vũ trụ song song bao gồm mọi thứ tồn tại, bao gồm toàn bộ vật chất, toàn bộ các định luật vật lí, và các hằng số cơ bản của tự nhiên. Muốn tham khảo thêm, quý độc giả có thể tìm đọc sách của Martin Ree nêu ở Danh mục tham khảo.
Điều đó đề xuất rằng cơ học lượng tử chưa phải là lí thuyết cuối cùng, mà chỉ là một gần đúng rất tốt cho thực tại vật chất ở những cấp độ rất nhỏ và với các định luật rất khác nhau mô tả các vật thể vĩ mô. Thế giới vi mô và vĩ mô dường như biệt lập với nhau. Thế nhưng cũng quả thật là các vật thể vĩ mô được làm từ số lượng lớn các thực thể lượng tử, và điều hợp lí là hỏi xem đường ranh giới nằm ở đâu? Mới đây, thí nghiệm hai khe đã được thực hiện với các phân tử khá lớn, các quả bóng bucky, thay cho electron. Các chùm phân tử C60 này (mỗi phân tử nặng gấp một triệu lần một electron) biểu hiện các hiệu ứng chồng chất lượng tử và giao thoa.
Một phương diện của thế giới lượng tử đặc biệt ma quái. Các thực thể lượng tử có thể đi xuyên qua những rào cản tưởng chẳng thể xuyên thủng như thể chúng là những bóng ma, một hiện tượng gọi là sự chui hầm lượng tử. Ảnh chụp STM ở Hình 4 được tạo ra bởi sự chui hầm lượng tử của các electron giữa một kim dò nhọn và các nguyên tử carbon nằm bên dưới đầu dò. Theo cổ điển, các electron không có đủ năng lượng để trèo qua hàng rào năng lượng tại đỉnh nhọn của đầu dò. Tuy nhiên, có một hình thức khác của nguyên lí bất định (DE. Dt ³ h/4p) kết nối sai số của một cặp biến bổ sung khác, năng lượng (DE) và thời gian (Dt). Điều này cho phép một hạt lượng tử vay mượn năng lượng DE mà nó cần để vượt qua một hàng rào năng lượng, miễn là nó trả lại món vay trong một thời gian Dt bị chi phối bởi nguyên lí bất định. Trong thế giới lượng tử, sự bảo toàn năng lượng có thể bị vi phạm, miễn đó là một vi phạm trong tíc tắc và khoản vay được trả lại đầy đủ. Giao dịch này cho phép các hạt lượng tử mở rộng sang các vùng bị cấm theo cổ điển và đi qua các hàng rào thế.
Sự chui hầm lượng tử xảy ra khi các hạt alpha được giải phóng bởi các hạt nhân phóng xạ, và giữa các proton trong lõi nóng của các sao. Khi hai proton tiến đến gần nhau, chúng chịu một lực đẩy tĩnh điện lớn, cố đẩy chúng ra xa. Tuy nhiên, bản chất dạng sóng của chúng cho phép chúng mở rộng và chui hầm qua khe trống, mang chúng đến đủ gần cho lực hạt nhân mạnh hợp nhất chúng với nhau và giải phóng năng lượng nhiệt hạch. Không có sự chui hầm lượng tử, các sao sẽ không tỏa sáng, và chúng ta sẽ không tồn tại.
Vật chất và lực
Trong thế giới hằng ngày, chúng ta xem những vật thể nhất định là giống hệt nhau. Ví dụ là các quả billard có cùng khối lượng, kích cỡ, và thành phần. Bóng billard có thể dễ dàng được đánh dấu, ví dụ bằng cách sơn cho chúng màu sắc khác nhau, để khi chúng chuyển động trên bàn billard lúc chơi, người ta theo dõi được đường đi của chúng. Trong thế giới lượng tử, khái niệm các hạt giống hệt và không thể phân biệt có một ý nghĩa khác và chặt chẽ hơn không cho phép chúng được đánh dấu. Hai hạt lượng tử được xem là y hệt nhau nếu các tọa độ hàm sóng của chúng có thể tráo đổi mà không gây ra bất kì thay đổi nào về đặc tính.
Trong thí nghiệm hai khe, chẳng hạn, nếu chúng ta cố khám phá xem electron đi qua khe nào, thì việc quan sát làm cho sóng vật chất lượng tử của nó không còn đồng bộ với chính nó (mất kết hợp) và vì thế hình ảnh giao thoa dạng sóng trên màn thủy tinh bị phá hủy. Tác dụng quan sát tương đương với việc đánh dấu một thực thể lượng tử, điều tự nhiên ngăn cấm. Quỹ đạo của những hạt lượng tử y hệt nhau là không thể quan sát được. Không giống các quả billard, các electron không thể được sơn những màu khác nhau.
Các hạt không thể phân biệt và y hệt nhau liên quan với cách vật chất và lực được phân biệt ở cấp cơ bản. Ở cấp con người, chúng ta thường cảm nhận vật chất và lực là những thứ khác nhau. Vật chất rõ là thứ gì đó sờ mó được, còn lực là phương thức của tự nhiên để khối vật chất này đẩy hoặc lấy hút khối vật chất khác ở lân cận. Tuy nhiên, trong thế giới vi mô, bản thân các lực được mang bởi các hạt. Tất cả các hạt của thế giới vi mô thuộc về một trong hai họ lớn: fermion và boson. Các hạt vật chất là fermion và các hạt mang lực là boson, chúng trung chuyển lực. Hai loại hạt cơ bản có tên gọi của chúng từ các quy luật thống kê mà chúng tuân theo khi số lượng lớn những hạt giống nhau kết hợp cùng nhau. Fermion, mang tên nhà vật lí Italy Enrico Fermi, tuân theo thống kê Fermi-Dirac còn boson, mang tên nhà vật lí Ấn Độ Satyendra Nath Bose, tuân theo thống kê Bose-Einstein.
Sự đối xứng giữ một vai trò trọng yếu trong việc phân biệt fermion với boson. Trong một hệ gồm những hạt y hệt nhau, xác suất Ψ2 không thể thay đổi nếu hoán đổi hai hạt bất kì trong số chúng. Khi hoán đổi một cặp hạt, điều này dẫn tới hai khả năng: hoặc là dấu của hàm sóng thay đổi (Ψ → − Ψ), trong trường hợp đó các hạt là fermion và có hàm sóng phản đối xứng, hoặc là dấu không đổi (Ψ → Ψ), và các hạt là boson với hàm sóng đối xứng.
Fermion và boson có các tính chất rất khác nhau. Khi các fermion cụm lại với nhau, chúng tránh chia sẻ trạng thái lượng tử của nhau và thay vậy chúng ưa phân tán trên thang mức năng lượng lượng tử, chiếm đầy các trạng thái sẵn có từ trạng thái cơ bản trở lên (Hình 17). Nếu có thêm một fermion gia nhập đám đông, nó phải chiếm giữ một thanh cao hơn của thang năng lượng và mảnh vật chất kết hợp chiếm giữ thể tích lớn hơn. Sự bất khả của các fermion trong việc chia sẻ cùng một trạng thái lượng tử cản trở các electron trong một nguyên tử tiến đến quá gần trạng thái của láng giềng của chúng, và gây ra nhiều tính chất của vật chất, ví dụ như sự kiên cố của nó. Mặt khác, các boson chẳng quan tâm các trạng thái bị chiếm giữ bởi boson khác, và còn ưa chiếm giữ cùng mức trạng thái cơ bản. Photon là boson. Bên trong mỗi máy hát đĩa compact là một laser, trong đó số lượng lớn boson tạo thành một trạng thái dạng sóng kết hợp với toàn bộ sóng lượng tử dao động hoàn toàn đồng bộ, giống như một binh đoàn đang trình diễn đi đều bước. Các chùm laser có thể được làm cho mạnh như yêu cầu bằng cách bổ sung thêm nhiều photon.
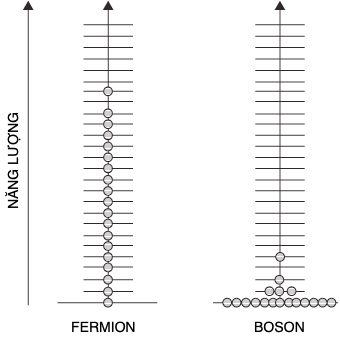
Hình 17. Tất cả các hạt trong vũ trụ hoặc là fermion hoặc là boson. Các hạt vật chất là fermion và các hạt mang lực là boson. Các hạt lượng tử y hệt nhau cụm lại với nhau trên thang mức năng lượng theo loại của chúng; các fermion tụ tập với mỗi hạt ở một trạng thái, còn các boson ưa suy sụp vào trạng thái cơ bản năng lượng thấp nhất.
Cái xác định một hạt là boson hay fermion liên quan đến một trong những tính chất lượng tử bí ẩn và khó hiểu nhất: spin. Các hạt lượng tử có thể có một moment động lượng nội tại như thể chúng đang quay tròn xung quanh một trục. Không có thứ tương đương chính xác nào cho spin lượng tử trong vật lí cổ điển. Thứ tương đương cổ điển gần gũi nhất cho spin là chuyển động tự quay, chẳng hạn chuyển động tự quay của Trái Đất quanh trục của nó. Nhưng đây là một cái bẫy. Trái Đất quay tròn một góc 360o quanh trục của nó trong hai mươi bốn giờ và vào hai ngày liên tiếp Mặt Trời mọc lên hầu như cùng lúc. Thế còn một hạt lượng tử, nó phải quay một góc bao nhiêu để nó trông y như cũ? Giống như bất kì vật quen thuộc nào, một boson có thể quay 360o để thỏa mãn yêu cầu này. Một fermion, mặt khác, phải quay gấp đôi (720o) thì mọi thứ mới trông như cũ được. Cứ như thể Trái Đất phải quay hai vòng, cho đến lúc mặt trời mọc lần tiếp theo. Thật lạ lùng làm sao!
Mỗi fermion là một hạt có spin lẻ bán nguyên (như 1/2, 3/2,…), còn mỗi boson có spin nguyên (0, 1, 2,…). Spin của một số boson và fermion được cho trên Bảng 1. Số lượng fermion trong vật chất bình thường được bảo toàn (ngoại trừ khi bị phân hủy bởi các hạt phản vật chất, chúng ta sẽ bàn tới ở Chương 6). Còn các boson không có giới hạn như thế; chúng được tạo ra và phân hủy với số lượng vô số bởi một tác dụng đơn giản như bật và tắt ánh sáng.
Bảng 1. Tính chất của một số boson và fermion.
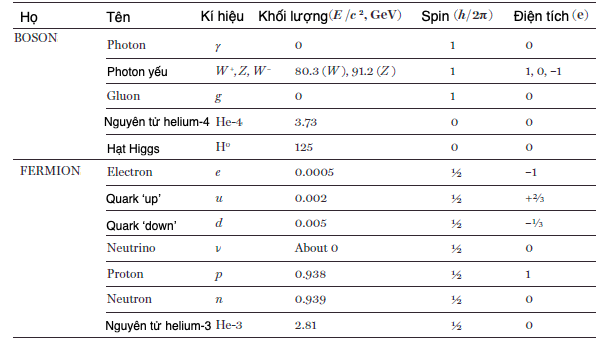
Nói boson trung chuyển lực giữa các hạt vật chất có nghĩa là gì? Hãy hình dung hai người trượt băng, trên mặt băng không ma sát. Khi họ trượt về phía nhau, một người ném một quả bóng nặng cho người kia chụp. Họ đều chuyển động theo chiều mới, động lượng và năng lượng được bảo toàn trong trao đổi vừa rồi. Một nhà quan sát ở xa cũng quan sát hai người trượt băng nhưng vì ở quá xa nên không nhìn thấy quả bóng mà chỉ thấy sự thay đổi chuyển động của họ. Nhà quan sát đó sẽ kết luận rằng hai người trượt băng đã tương tác thông qua một lực. Trong ví dụ tương đương này, hai người trượt băng tiêu biểu cho các hạt vật chất fermion và quả bóng là một boson trung chuyển lực. Sự trao đổi một hạt minh họa cách các lực hoạt động trên cấp vi mô; tuy nhiên, các ví dụ tương đương vĩ mô của thế giới lượng tử nên luôn xem xét thận trọng.
Các boson trung chuyển lực giữa các hạt vật chất bằng cách thoắt ẩn thoắt hiện dưới dạng các hạt ảo; đây là những ‘quả bóng nặng’ của thế giới vi mô. Chúng ta sẽ thấy vai trò trung tâm của chúng đối với vật chất ở Chương 7. Một photon ảo vận hành như thế nào? Trong khoảnh khắc tồn tại ngắn ngủi của nó, một photon ảo vay mượn năng lượng của nó từ chân không, như được phép bởi nguyên lí bất định Heisenberg. Sự tồn tại phù du của các hạt ảo có nghĩa là ngay cả một hệ năng lượng zero cũng tự phát tạo ra các hạt giàu năng lượng. Khi hai electron đẩy lẫn nhau, lực điện từ giữa chúng được mang bởi một photon ảo, một boson vector spin-1. Hạt được gọi là boson vector do nó là lượng tử của một trường vector, và có ba chiều không gian khả dĩ trong đó trục spin của hạt có thể định hướng. Cơ học lượng tử cấm một hạt ảo được quan sát. Hoặc là lượng tử ảo phải được hấp thụ toàn bộ bằng cách nhận lấy hạt hoặc là không.
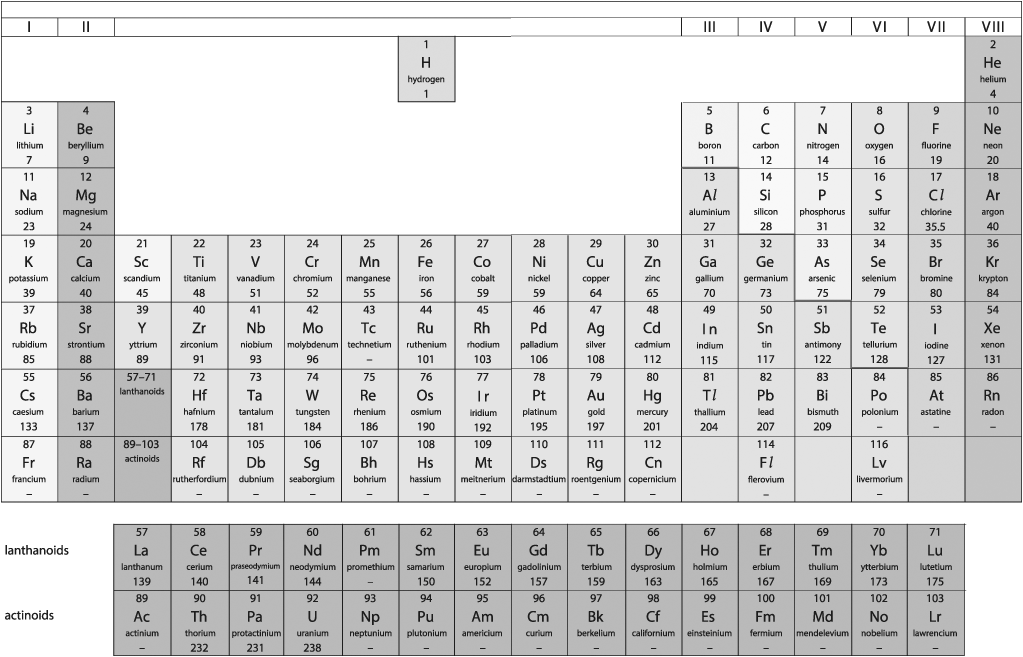
Cấu trúc của bảng tuần hoàn
Một trong những thành tựu vĩ đại nhất của cơ học lượng tử là nó giải thích được cấu trúc của bảng tuần hoàn. Khi áp dụng phương trình Schrödinger cho nguyên tử, nó dự đoán các hàm sóng electron đại diện cho những loại sóng dừng khác nhau. Đây được gọi là các orbital và vạch rõ vùng không gian trong đó một electron có khả năng được tìm thấy cao nhất. Một orbital nguyên tử được đặc trưng bởi bốn số lượng tử, chúng xác định một số hình dạng orbital khác nhau trong không gian ba chiều. Hàm sóng cho trạng thái cơ bản của nguyên tử hydrogen là một quả cầu, với một cực đại ở gần hạt nhân, dần dần giảm theo bán kính (Hình 18). Nhưng ở một trạng thái kích thích, electron dành nhiều thời gian hơn ở xa hạt nhân. Một số kiểu sóng năng lượng cao hơn này có dạng giống như các quả cầu rỗng, với một cái lõi ở giữa, và một số khác thì có hình quả tạ với hai cái thùy có tâm trên hạt nhân. Có ba định hướng khả dĩ cho quả tạ đó, mỗi quả định hướng cho một chiều trong không gian, chúng có năng lượng bằng nhau. Các trạng thái có năng lượng cao hơn thì có phân bố mật độ electron phức tạp hơn.
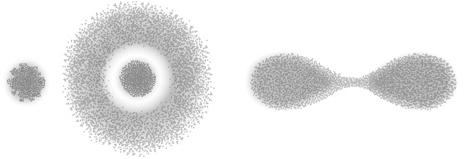
Hình 18. Các phân bố mật độ electron hình cầu và hình quả tạ cho trạng thái cơ bản của hydrogen (trái) và một số trạng thái kích thích. Mật độ biểu diễn kiểu sóng, và lượng thời gian electron cư trú ở một điểm cho trước ở gần hạt nhân ở giữa.
Các electron lấp đầy các mức nguyên tử từ trạng thái cơ bản trở lên. Vào năm 1925, Wolfgang Pauli đã khám phá nguyên lí chi phối cách electron lấp đầy các trạng thái. Nếu tráo đổi hai electron ở cùng một trạng thái, thì Ψ không thể thay đổi. Vì electron là fermion, nên điều này ngụ ý rằng Ψ = 0, nói cách khác có xác suất zero để hai electron chiếm giữ cùng một trạng thái. Đây là nguyên lí loại trừ Pauli, nguyên lí giữ vai trò then chốt trong cấu trúc nguyên tử và gây ra cấu trúc giống lớp vỏ của các nguyên tố thuộc bảng tuần hoàn, tạo nên các nhóm với 2, 8, 8, 18,… thành viên.
Khi hình thành nên các nguyên tử vượt quá hydrogen, các phân bố đám mây electron tương tự như các minh họa ở Hình 18 nhưng, do có điện tích hạt nhân lớn hơn, nên các đám mây electron bị hút vào chặt hơn. Nguyên tố tiếp theo trên bảng tuần hoàn là helium, với hai proton trong hạt nhân. Nguyên lí Pauli cho phép electron ghép cặp spin, với một spin ‘up’ và một spin ‘down’, tiến vào trạng thái cơ bản để hình thành lớp vỏ bền đầu tiên trong nguyên tử. Ở helium, các đám mây electron tạo nên một quả cầu chắc gọn hơn ở hydrogen, và điều này được phản ánh ở năng lượng ion hóa cao hơn của nó, bằng 24,6 eV, gần gấp đôi so với hydrogen.
Nguyên tố tiếp theo trên bảng tuần hoàn, lithium, có ba proton. Electron thứ ba bị loại trừ, không thể gia nhập với bộ đôi trong lớp vỏ đầu tiên và thay vậy nó phải đi vào trạng thái năng lượng cao tiếp theo sẵn có, và bắt đầu một lớp vỏ mới dưới dạng một electron hóa trị. Tại đó, nó ở xa hạt nhân hơn và một phần được che chắn khỏi điện tích hạt nhân bởi đám mây electron phía trong. Điều này khiến lithium có hoạt tính hóa học mạnh hơn và dễ dàng bị ion hóa, dấu hiệu của các nguyên tố tạo nên dải kim loại. Đa số nguyên tố trong bảng tuần hoàn là kim loại. Các phi kim chủ yếu được tìm thấy ở bên phải phía trên một đường chéo chạy từ boron xuống astatine.
Một đặc điểm nổi bật của bảng tuần hoàn là tính tuần hoàn ‘quãng tám’ của nó. Tính chất này phát sinh từ việc có bốn hình dạng cơ bản của các orbital nguyên tử: một hàm sóng hình cầu và ba quả tạ, mỗi quả tạ cho một chiều không gian. Mỗi orbital này có thể nhận một cặp electron spin đối song, tạo ra tám trạng thái trong một lớp vỏ hoàn chỉnh. Vì thế, khi di chuyển theo hàng ngang sang cột tiếp theo của bảng tuần hoàn, từ lithium sang neon, tám electron được thêm từng electron một để cân bằng với điện tích hạt nhân. Neon có lớp vỏ đầy gồm tám electron, khiến nó là một khí hiếm trơ về mặt hóa học, giống như helium. Vượt quá neon là nguyên tố sodium hoạt tính; electron hóa trị thêm vào phải bắt đầu một lớp vỏ mới, và vì thế quá trình lặp lại.
Trong chương này, chúng ta đã nhìn vào những khám phá nổi bật hồi đầu thế kỉ 20 làm bộc lộ cấu trúc bên trong của nguyên tử, và nền vật lí mới mang tính cách mạng phát triển song hành với chúng: cơ học lượng tử. Hạt nhân nguyên tử rất nhỏ, khiến nguyên tử chủ yếu là không gian trống rỗng, cư trú trong đó là trường điện từ hút lấy các electron trong các lớp vỏ lượng tử của chúng. Hạt nhân chứa hai loại hạt, proton và neutron, chúng được liên kết với nhau bằng lực hạt nhân mạnh tầm ngắn. Trường điện từ trơn mượt và liên tục mà Maxwell hình dung thật ra được làm từ những bầy đoàn gồm vô số lượng tử. Ranh giới phân chia giữa thế giới lượng tử và thế giới vĩ mô được đánh dấu bởi kích cỡ của một hằng số cơ bản của tự nhiên – hằng số Planck. Nguyên lí bất định Heisenberg chi phối hành trạng của thế giới vi mô, và cho thấy các hạt có thể chui hầm như thế nào qua các hàng rào không thể vượt qua theo lí thuyết cổ điển. Vũ trụ chứa hai loại hạt, fermion và boson. Fermion là các hạt vật chất, và boson là các hạt mang lực. Chỉ có một fermion có thể chiếm giữ một trạng thái lượng tử cho trước, đó là lí do vì sao vật chất fermion chiếm giữ không gian. Mặt khác, các boson ưa tụ tập vào cùng một trạng thái lượng tử trong đó chúng có thể tạo nên các trường kết hợp. Thành công to lớn của thuyết lượng tử là nó giải thích được cấu trúc của bảng tuần hoàn, các tính chất của nguyên tử, phân tử, các vật liệu, và bản thân sự sống.
Mặc dù các tính chất lượng tử của vật chất chủ yếu ràng buộc với các cấp vi mô, nhưng thỉnh thoảng chúng có thể tự biểu hiện trên vĩ mô. Ở Chương 6 chúng ta sẽ tìm hiểu cách các đám gồm rất nhiều hạt có thể biểu hiện những hiệu ứng lượng tử vĩ mô.
TÌM HIỂU NHANH VỀ VẬT CHẤT
Geoff Cottrell (Oxford University Press 2019)
Bản dịch của Thuvienvatly.com
MỤC LỤC
4 Năng lượng, khối lượng, và ánh sáng
5 Thế giới lượng tử của nguyên tử
9 Vật chất tối và năng lượng tối