Chlorine
Nhanh chóng và chết chóc, nguyên tố số 17 chưa bao giờ có thể giải phóng nó ra khỏi chiến trận. Bị nhà hóa học Đức Fritz Haber cáo buộc là ‘hình thức giết người cao cấp’, khí chlorine được sử dụng trên các chiến trường Thế chiến Thứ nhất: chính những tính chất biến nó thành chất làm sạch cực mạnh và chất tẩy trắng đã biến nó thành một thứ vũ khí khủng khiếp. Hít vào trong phổi, halogen cực kì hoạt tính này tàn phá các mô tế bào mong manh, làm cho nạn nhân đắm chìm trong máu của chính họ. Lành tính hơn, người ta có thể dùng chlorine tiêu diệt các mầm bệnh trong nước, lọc nước để uống hoặc dùng trong hồ bơi.
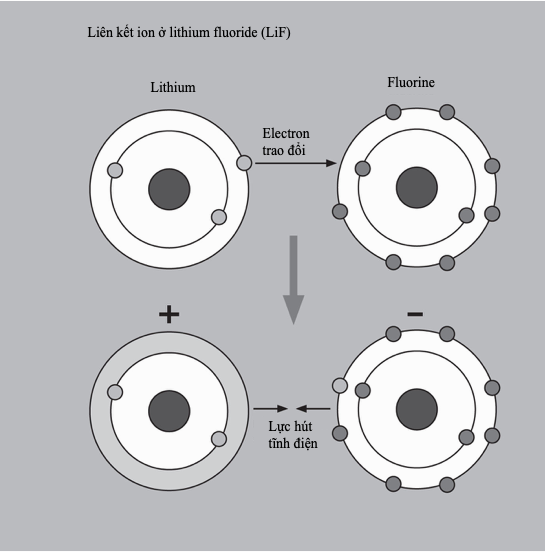
Dưới các điều kiện bình thường, chlorine là một chất khí lưỡng nguyên tử màu vàng lục. Các nguyên tử chlorine độc thân có độ âm điện cao và lập tức tạo nên các muối ion, ‘đánh cắp’ một electron từ nguyên tử khác để lấp đầy lớp vỏ ngoài cùng của chúng. Muốn quan trọng nhất là sodium chloride (muối ăn, natri clorua), nó giữ một vai trò thiết yếu trong cơ thể. Chlorine còn có mặt trong nhiều hợp chất công nghiệp quan trọng, có thể kể như acid hydrochloric, các plastic như PVC và thuốc trừ sâu DDT.

Argon
Mặc dù thường bị xem nhẹ và có tên gọi nghĩa là ‘lười biếng’, thế nhưng argon chiếm ngót nghét 1 phần trăm khí quyển Trái Đất. Con số đó tương đương chừng 50 nghìn tỉ tấn khí trôi nổi trong không khí, và khiến nó là nguyên tố khí quyển dồi dào thứ ba sau nitrogen và oxygen.
Là một chất khí hiếm tiêu biểu, argon gần như hoàn toàn trơ ì, và do đó trạng thái bình thường của nó là ở dạng nguyên tố, đơn nguyên tử. Tuy nhiên, sự trơ ì của argon không khiến nó thành vô dụng – nó thường được dùng làm khí trơ an toàn bảo vệ cho những chất dễ nổ hay phản ứng nguy hiểm. Cùng với oxygen, nó còn được thổi bọt vào thép nóng chảy -argon khuấy trộn kim loại còn oxygen loại bỏ carbon ở dạng carbon dioxide. Argon được dùng để ngăn không khí và tránh oxy hóa khi hàn hồ quang trên nhôm và nuôi cấy tinh thể silicon siêu tinh khiết. Vào năm 2000, các nhà hóa học tại Đại học Helsinki cuối cùng đã thành công đưa argon tham gia vào một phản ứng; tuy nhiên, argon fluorohydride thu được là không bền ở nhiệt độ trên –246 ºC (-411 °F).

Bảng tuần hoàn hóa học tốc hành | Dan Green
Bản dịch của Thuvienvatly.com