Có hàng nghìn phiên bản khác nhau của bảng tuần hoàn đã được người ta sáng tạo ra kể từ khi Dmitri Mendeleev phác họa nó lần đầu tiên cách nay 150 năm – thế nhưng tại sao có một phiên bản lại quen thuộc với chúng ta hơn hết thảy?
- Robert P Crease (Physics World, tháng 2/2019)

Vào đầu năm 1869, nhà hóa lí người Nga Dmitri Mendeleev đang dần nản chí trong khi soạn tập hai của bộ giáo trình Các nguyên lí Hóa học của ông. Mặc dù tập một của ông dài đến 600 trang, nhưng Mendeleev chỉ mới bao quát được vỏn vẹn 8 trong chừng 60 nguyên tố đã biết.
Trước kì hạn nộp quyển tiếp theo cho nhà xuất bản rồi vui vẻ đi châu Âu, ông quyết định phác thảo một cái bảng, đặt các nguyên tố vào các cột và các hàng, xếp trật tự chúng bởi trọng lượng nguyên tử theo một cách thể hiện các tương đồng hóa tính của chúng. Ông lập bảng vào ngày 17 tháng Hai theo lịch Julian sử dụng ở nước Nga khi ấy (tương ứng với ngày 1 tháng Ba theo lịch Grogorian sử dụng trên khắp châu Âu).
Mendeleev không hẳn hài lòng với cái bảng này, và ông vẫn tiếp tục sáng tạo thêm chừng 60 phiên bản nữa của nó. Thế nhưng cái bảng ngày 17 tháng Hai của ông đã trở thành nền tảng cho bảng tuần hoàn ngày nay có mặt trong các trang sách của mỗi quyển giáo khoa hóa học và được treo trong hầu như mỗi lớp học hóa trên khắp thế giới. Vậy tại sao bảng này lại nổi đình nổi đám, chứ không phải hàng nghìn phiên bản khác mà người ta có thể tìm thấy trong Cơ sở dữ liệu Internet về Bảng Tuần hoàn? Nó bao gồm nhiều bảng trông không những tương tự mà còn có các bảng xoắn ốc, bảng tròn, và cả bảng 3D. Câu trả lời chuẩn, theo sách vở là rằng bảng của Mendeleev là bảng đầu tiên được cố gắng vẽ ra nhằm thể hiện các liên hệ hóa tính giữa mọi nguyên tố đã biết được xếp trật tự theo trọng lượng nguyên tử. Thế nhưng lí do thực tế thì phức tạp hơn.
Một người có câu trả lời là Ann Robinson, một nhà nghiên cứu lịch sử khoa học làm việc trong Thư viện Widener tại Đại học Harvard ở Mĩ. Robinson cách người đầu tiên nghiên cứu lịch sử bảng tuần hoàn một khoảng cách thế hệ rất xa, song cô là một trong những người mới đây nhất có luận án tiến sĩ về đề tài này hồi năm ngoái từ Đại học Massachusetts ở Amherst. Luận án của cô thật hợp thời: tháng này là kỉ niệm 150 năm ra đời bảng tuần hoàn 17 tháng Hai của Mendeleev, và tháng Bảy tới sẽ tròn một trăm năm của Hiệp Hội Hóa họa và Hóa học Ứng dụng Quốc tế (IUPAC), tổ chức giám sát danh pháp toàn cầu và các tiêu chuẩn trong hóa học.
Vấn đề cân nặng
Gần đây tôi có đến thăm Robinson tại Widener, trái tim địa lí và trí tuệ của khu trường sở Harvard. Gặp tôi trong hành lang của tòa nhà uy nghi, nhiều hàng cột này, Robonsin cho tôi xem một trong những báu vật của thư viện trường – một quyển Kinh thánh Gutenberg, được trưng bày nổi bật trong một cái hộp nhiều hoa văn, đó là một trong 49 bản sao còn sót lại của quyển sách có nhiều giá trị lịch sử này.
Vào thập niên 1860, Robinson lí giải, các nhà hóa học đã làm rõ được rằng trọng lượng nguyên tử là đặc trưng quan trọng nhất để xếp trật tự các nguyên tố. Một số nhà hóa học còn lưu ý rằng, khi xâu chuỗi theo cách đó, các nhóm nguyên tố có các tính chất giống nhau. Vài người đã thử biểu diễn góc nhìn này một cách có hệ thống, bao gồm nhà khoa học Anh John Newlands. Trình bày trong một loạt bài báo ngắn công bố trên tạp chí Chemical News vào đầu những năm 1860, ông đề xuất – và minh họa bằng hình ảnh – một “quy tắc quãng tám”, nguyên lí của nó là cứ mỗi nguyên tố thứ tám trong danh sách của ông biểu hiện hành trạng hóa học giống nhau. Song những người khác nhạo báng quy tắc ấy của Newlands, với nhiều nhà hóa học cho rằng ông chỉ là mèo mù vớ cá rán. Cũng chẳng có ích lợi gì khi Newlands so sánh các liên hệ nguyên tố ấy với các nốt của quãng tám trong âm nhạc, một liên hệ có vẻ kì cục đối với mọi người, trừ bản thân Newlands.
Trong khi đó, ở nước Nga, và ban đầu chẳng hay biết gì về công trình của Newlands, Mendeleev đang làm việc tại Đại học St Petersburg, nơi ông vừa được bổ nhiệm chức danh giáo sư vào năm 1864. Ông cảm thấy thất vọng trước các quyển giáo trình hóa học hiện có, chúng phân chia các nguyên tố thành hoặc là kim loại hoặc là phi kim và phân loại chúng bởi “hóa trị” của chúng, hay khả năng kết hợp với các nguyên tố khác. Như nhà nghiên cứu lịch sử khoa học tại Đại học Princeton, Michael Gordin, thuật lại trong quyển sách mới tái bản của ông: Một trật tự đẹp: Dmitri Mendeleev và Cái bóng của Bảng tuần hoàn, Mendeleev quyết tâm viết giáo trình của riêng ông, gửi Tập 1 cho nhà xuất bản vào tháng Giêng 1869.
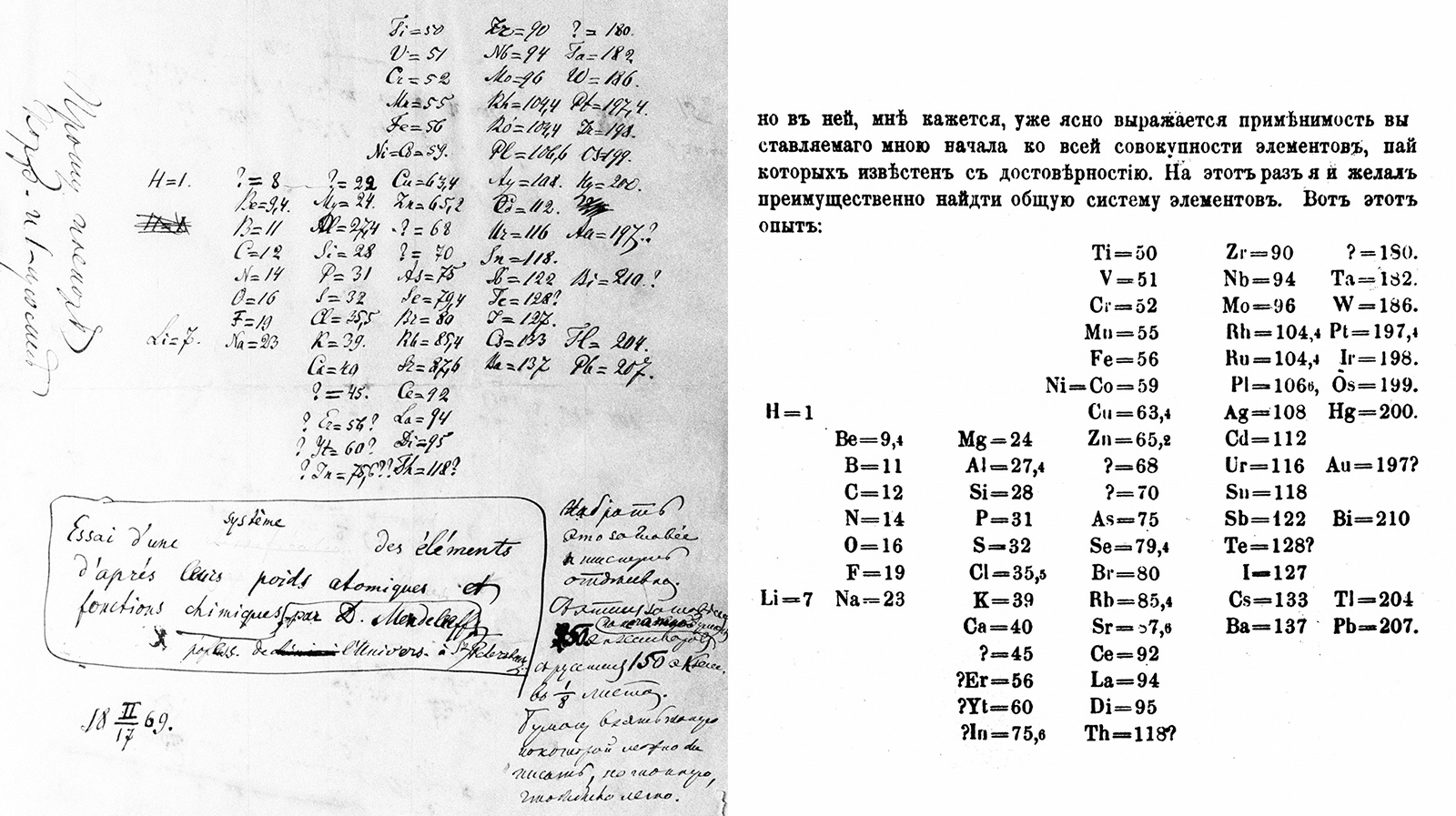
Bảng tuần hoàn viết tay của Dmitri Mendeleev (trái) được soạn vào ngày 17 tháng Hai 1869 và hầu như không thể nhận ra với phiên bản mà chúng ta biết và yêu thích ngày nay. Phiên bản bên phải được xuất bản trong bài báo khoa học đầu tiên của ông về bảng tuần hoàn. Để có cái na ná với bảng tuần hoàn hiện đại, bạn phải hình dung quay sơ đồ này 90o theo chiều kim đồng hồ và rồi đảo các nguyên tố từ trái thành phải. (Ảnh: Sputnik/Science Photo Library; Universal History Archive / UIG / Science Photo Library)
Thế nhưng mới chỉ bao quát có tám trong 63 nguyên tố đã biết, Mendeleev bắt đầu cô đọng nội dung trình bày của ông trong Tập II trước hạn nộp bài đang đến gần và số trang hạn chế, ông cố gắng làm sáng tỏ các nguyên tố còn lại theo một cách sẽ thể hiện các liên hệ của chúng. Và thế là vào ngày 17 tháng Hai 1869 Mendeleev gửi cho Hội Hóa học Nga một sơ đồ một mặt giấy, tựa đề là “Một nỗ lực nhằm hệ thống các nguyên tố, dựa trên trọng lượng nguyên tử và các tương đồng hóa tính của chúng”.
Sơ đồ ấy, Gordin cho biết, “nảy sinh từ nhu cầu về một ‘sự phân loại’ mang tính sư phạm [để] trình bày nội dung kiến thức với sinh viên hóa học mới nhập môn”. Sau đó Mendeleev đăng kí một bài báo với hội và trong năm 1869 ông công bố một bài tóm tắt về nó cùng với một phiên bản của bảng tuần hoàn trên tạp chí Zeitschrift für Chemie (12 405).
Robinson rút ra một bản sao sơ đồ gốc của Mendeleev. Gồm sáu cột lung tung từ hai đến 19 nguyên tố, nó trông chẳng giống tẹo nào với bảng tuần hoàn hiện đại mà chúng ta biết và yêu thích. “Anh phải xoay nó 90o theo chiều kim đồng hồ, và tưởng tượng các nguyên tố đảo từ trái sang phải, thì toàn bộ bảng tuần hoàn sẽ hiện ra,” cô ta giải thích. Khi tôi làm thế, quả thật nó trông na ná như bảng tuần hoàn quen thuộc của chúng ta.
Lấp vào chỗ trống
Thế nhưng Mendeleev vẫn chưa hài lòng với sơ đồ mới của ông. Một đặc điểm phiền phức, Robinson giải thích, là trong một vài trường hợp, việc bố trí các nguyên tố theo hành trạng hóa học của chúng xung đột với vị trí của chúng xếp theo trọng lượng nguyên tử. Tellurium (Te) chẳng hạn, Mendeleev do dự gán cho nó trọng lượng nguyên tử “128?”, phải xếp trước iodine (I), nó có trọng lượng nguyên tử 127. (Ngày nay chúng ta biết rằng trọng lượng nguyên tử cho Te là 127,6 và cho I là 126,9).
Một đặc điểm khó hiểu nữa, theo Robinson, là cái bảng ấy đúng theo nghĩa đen là có những chỗ trống mà Mendeleev đã chèn vào các dấu hỏi. Ở bảng tuần hoàn công bố cùng với bài tóm tắt, các vị trí này là cho các nguyên tố nằm bên dưới boron (B), nhôm (Al), manganese (Mn), và silicon (Si) – cái gọi là các nguyên tố đất hiếm, với trọng lượng nguyên tử xấp xỉ 45, 68, 70 và 180. Mendeleev cho rằng các chỗ trống này chẳng phải do sự không thỏa đáng trong sơ đồ phân loại của ông, mà chúng sẽ được lấp đầy bởi các nguyên tố chưa được khám phá cho đến khi ấy. Thật vậy, Mendeleev còn tin chắc vào sự tồn tại của các nguyên tố mới ấy đến mức ông đã mô tả hành trạng hóa học của chúng và đặt tên cho chúng bằng cách gán thêm tiếp ngữ “eka” (từ tiếng Sanskrit chỉ “proto”) vào tên những nguyên tố mà chúng có biểu hiện giống nhất. Nguyên tố bên dưới nhôm, chẳng hạn, được đặt tên là eka-nhôm.

Dmitri Mendeleev (1832 – 1907) là người có tầm nhìn xa rộng ở chỗ bảng tuần hoàn của ông đã dự đoán bốn nguyên tố sau này được tìm thấy: gallium, scandium, germanium, và technetium. (Ảnh: Sputnik/Science Photo Library)
Một đặc điểm gây hiếu kì nữa của bảng tuần hoàn của Mendeleev ngày ấy, đối với chúng ta, là một chỗ được chiếm giữ bởi một nguyên tố ghi là “Di” với trọng lượng nguyên tử bằng 95. Như Robinson giải thích với tôi, kí hiệu đó chỉ didymium, về sau hóa ra không phải một nguyên tố mà là một kết hợp của praseodymium (Pr) với neodymium (Nd). Dù vậy, nó là một chất có thật, dùng trong kính bảo vệ chặn ánh sáng màu vàng.
Hậu thuẫn đầu tiên cho tầm nhìn của Mendeleev xảy đến vào năm 1875 khi nhà hóa học Pháp Paul Émile Lecoq de Boisbuadran tìm thấy eka-nhôm, ông đặt lại tên cho nó là gallia (nhằm tôn vinh tên gọi Latin cho vùng Gaul) – trong tiếng Anh hiện đại là gallium (Ga). Kết quả ấy khiến người ta chú ý đến sơ đồ của Mendeleev, tuy rằng đa số các nhà hóa học vẫn chưa bị thuyết phục hẳn. Như Robinson cho biết, dự đoán này được xem là “một may mắn tình cờ, một cú ăn may”.
Thế rồi, bốn năm sau, nhà hóa học Thụy Điển Lars Fredrik Nilson tìm thấy eka-boron – cái ngày nay chúng ta gọi là scandium (Sc). “Lẽ nào ông ta may mắn hai lần?” Robinson lí luận. “Người ta nghĩ, ‘rốt cuộc có gì đó chăng!” Mang tính thuyết phục hơn nữa là Mendeleev không chỉ dự đoán các nguyên tố này, mà ông còn dự báo chính xác hóa tính và trọng lượng nguyên tử của chúng. Bằng chứng tiếp sau đó ủng hộ cho bảng tuần hoàn của ông xuất hiện vào năm 1886 khi eka-silicon (nay gọi là germanium, Ge) được tìm thấy, mặc dù thế giới phải chờ đến năm 1937 mới tìm thấy eka-manganese, nguyên tố ngày nay được gọi là technetium (Tc) và là một trong các nguyên tố có các đồng vị thiết yếu trong vật lí y khoa.
123physics dịch từ tạp chí Physics World, số tháng 2/2019


![[LỚP 10] Sách Bứt Phá 9+ Lớp 10 Phòng luyện Topclass Toán hoặc Văn Combo bứt phá điểm cao HOCMAI](https://thuvienvatly.com/images/deals/thumb/lop-10-sach-but-pha-9-lop-10-phong-luyen-topclass-toan-hoac-van-combo-but-pha-diem-cao-hocmai.jpg)