Câu hỏi
🗣️ Trần Thị Lộc hỏi: Cho mình hỏi một câu Đánh giá năng lực trong sách bài tập
Cho m gam hỗn hợp G gồm Mg và Al có tỉ lệ mol 4 : 5 vào dung dịch HNO3 20%. Sau khi các kim loại tan hết có 6,72 lít hỗn hợp X gồm NO, N2O, N2 bay ra (đktc) và được dung dịch T. Thêm một lượng O2 vừa đủ vào X, sau phản ứng được hỗn hợp khí Y. Dẫn Y từ từ qua dung dịch KOH dư, có 4,48 lít hỗn hợp khí Z đi ra (đktc). Tỉ khối của Z đối với H2 bằng 20. Nếu cho dung dịch NaOH vào dung dịch T thì lượng kết tủa lớn nhất thu được là (m + 39,1) gam. Biết HNO3 dùng dư 20% so với lượng cần thiết. Nồng độ phần trăm của Al(NO3)3 trong T gần nhất với
(A) 9,7%
(B) 9,6%
(C) 9,4%
(D) 9,5%
👩 Đánh giá của giáo viên: Câu này dễ, mức độ biết.
🔑 Chủ đề: nitric acid.
Câu trả lời hay nhất
🕵 Bạn Phạm Thị Thành trả lời:
Chọn câu (A): 9,7%
Trả lời: Khi thêm O2 vừa đủ vào Y thu được các khí NO2, N2O, N2. Dẫn qua dung dịch KOH dư thì NO2 bị hấp thụ khí còn lại là N2O và N2. =>nNO = nNO2 = 0,3 – 0,2 = 0,1 mol Áp dụng đường chéo cho hỗn hợp Z: Mà nN2O + nN2 = nZ = 0,2 mol =>nN2O = 0,15 và nN2 = 0,05 Đặt: nMg = 4x và nAl = 5x (mol) =>nMg(OH)2 = 4x và mAl(OH)3 = 5x m kết tủa max = mKL + mOH- =>m + 39,1 = m + 17(4x.2 + 5x.3) =>x = 0,1 =>nMg = 0,4 mol và nAl = 0,5 mol Ta thấy: 2nMg + 3nAl >3nNO + 8nN2O + 10nN2 =>Có tạo muối NH4NO3 Bảo toàn e: 2nMg + 3nAl = 3nNO + 8nN2O + 10nN2 + 8nNH4NO3 =>2.0,4 + 3.0,5 = 3.0,1 + 8.0,15 + 10.0,05 + 8nNH4NO3 =>nNH4NO3 = 0,0375 mol Công thức tính nhanh: nHNO3pư = 4nNO + 10nN2O + 12nN2 + 10nNH4NO3 = 2,875 mol =>nHNO3bđ = 2,875 + 2,875.(20/100) = 3,45 mol =>m dd HNO3 = 3,45.63.(100/20) = 1086,75 gam m dd sau pư = mMg + mAl + m dd HNO3 – mNO – mN2O – mN2 = 0,4.24 + 0,5.27 + 1086,75 – 0,1.30 – 0,15.44 – 0,05.28 = 1098,85 gam Ta có: nAl(NO3)3 = nAl = 0,5 mol → %mAl = (0,5.213/1098,85).100% = 9,69% gần nhất với 9,7%
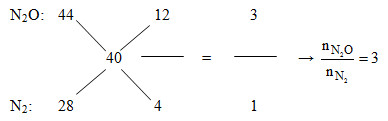
Câu trước | Câu kế tiếp
Các câu trả lời
👤 Trần Hậu Thành viết:
Chọn C, 9,4%
👤 Lê Trí Lộc viết:
Chọn D, 9,5%
👤 Phạm Trọng Phú viết:
Chọn B, 9,6%
👤 Lê Khanh Đức viết:
Chọn A, 9,7%
➥ 🗣️ Trần Thị Lộc trả lời: Cảm ơn bạn, câu này hình như có trong file doc này Đánh Giá Năng Lực - Nitric acid
👤 Lê Thị Ngọc viết:
Chọn A: 9,7%
Gửi bạn các file hữu ích đi kèm câu hỏi:


